유전자재조합 항원단백질 백신
질병청, 총 32만회분 순차적 도입
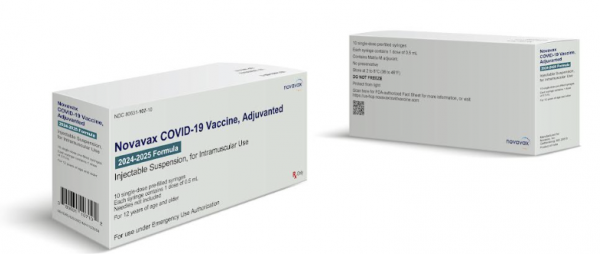
식품의약품안전처는 30일 미국 노바백스의 '코로나19 JN.1 변이 대응 백신(2024-2025 조성)'에 대해 긴급사용승인했다고 밝혔다.
긴급사용승인은 감염병 대유행 등 공중보건 위기 상황에 적절히 대응하기 위해 관계 중앙행정기관의 장의 요청이 있는 경우 식약처장이 제조·수입자에게 국내에 허가되지 않은 의료제품을 제조하거나 수입하게 해 공급하게 하는 제도다. 이번 긴급사용승인은 올해 동절기 코로나19 예방을 위한 백신 접종계획에 따라 질병관리청이 요청함에 따라 신속하게 검토 후 이뤄졌다고 식약처는 설명했다.
노바백스 코로나19 백신은 앞서 JN.1 변이 대응 백신으로 식약처 허가를 받은 화이자와 모더나 백신이 신체 면역반응을 유도하는 항원 단백질을 발현하는 mRNA(메신저 리보핵산)를 주성분으로 하는 것과 달리 바이러스를 제거하는 항체 생성을 유도하기 위해 유전자재조합 기술로 만든 항원 단백질을 직접 체내에 주입하는 백신이다.
안재용 SK바이오사이언스 사장은 "최근 코로나19 유행 상황이 급변하고 있는 시점에 국민들의 백신 선택권을 넓히게 됐다"며 "유일한 합성항원 방식인 노바백스 신규 변이 백신이 적기에 안정적으로 공급될 수 있도록 최선을 다할 것"이라고 말했다.
지금 뜨는 뉴스
이번 노바백스 백신은 SK케미칼에서 수입해 국내 공급하며, 질병관리청 등에 대한 공급은 SK케미칼의 자회사인 SK바이오사이언스가 담당한다. 식약처의 긴급사용승인에 따라 질병청은 이날 노바백스 JN1. 변이 대응 백신 10만회분을 도입했으며, 이후 이를 포함해 총 32만회분을 순차적으로 들여올 계획이다.
조인경 기자 ikjo@asiae.co.kr
<ⓒ투자가를 위한 경제콘텐츠 플랫폼, 아시아경제(www.asiae.co.kr) 무단전재 배포금지>







![전문가 4인이 말하는 '의료 생태계의 대전환'[비대면진료의 미래⑥]](https://cwcontent.asiae.co.kr/asiaresize/319/2026013014211022823_1769750471.png)










![데려올 때 38만원, 떠나보낼 때 46만…가슴으로 낳아 지갑으로 키우는 반려동물[펫&라이프]](https://cwcontent.asiae.co.kr/asiaresize/308/2026020509403529611_1770252035.jpg)





![[단독]'빗썸 비트코인 오지급' 법원판단 예고편 나왔다](https://cwcontent.asiae.co.kr/asiaresize/308/2026021309531941937_1770943999.jpg)
