[아시아경제 고형광 기자] 삼성바이오에피스가 자체 개발한 항체 바이오시밀러(바이오의약품 복제약)가 처음으로 미국에서 판매 허가를 받고 미국 시장에 본격 진출한다.
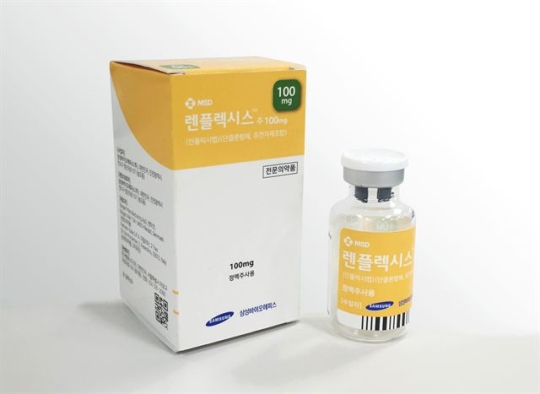
삼성바이오에피스는 21일(현지시간) 미국 식품의약국(FDA)로부터 자가면역질환 치료제 '렌플렉시스'(성분명 인플릭시맙)의 판매 허가 승인을 받았다고 22일 밝혔다.
렌플렉시스는 미국 제약사 존슨앤존슨의 항체의약품인 '레미케이드'의 바이오시밀러다. 지난해 전 세계적으로 연간 9조3000억원 이상 팔린 블록버스터 의약품이다. 류머티스 관절염, 궤양성 대장염, 크론병, 강직성 척추염, 건선성 관절염 및 건선 치료에 쓰인다.
삼성바이오에피스는 지난해 3월 미국 FDA에 렌플렉시스 판매 허가를 신청하고 13개월만에 승인 받았다.
국내에서는 2015년 승인 받았으며 유럽과 호주에서는 지난해 승인 받는 등 이번이 네번째 판매 승인이다.
삼성바이오에피스는 이번 승인으로 연구개발(R&D) 역량 및 제품이 국제적으로 인정받는 계기가 됨은 물론 세계 최대 바이오 의약품 시장인 미국에서 글로벌 제약사들과 경쟁할 수 있는 초석을 마련한 것으로 평가하고 있다.
미국에서의 판매는 삼성바이오에피스의 파트너사인 글로벌 제약사 머크가 담당하게 된다.
삼성바이오에피스의 고한승 사장은 "이번 미국 판매 허가 승인은 회사 창립 5년만에 이룬 쾌거이며 유럽에 이어 미국에서도 더 많은 자가면역 질환 환자들이 바이오의약품으로 치료 받을 기회를 가질 수 있을 것으로 기대된다"며 "이번 승인으로 현재 진행 중인 바이오시밀러의 매출 확대에 더욱 박차를 가할 것"이라고 말했다.
한편 삼성바이오에피스는 현재 엔브렐 바이오시밀러(성분명 에타너셉트)인 브렌시스를 호주, 캐나다, 한국, 유럽(유럽명 베네팔리)등에 판매 중이다.
또 휴미라(성분명 아달리무맙) 바이오시밀러, 허셉틴(성분명 트라스투주맙) 바이오시밀러는 EMA(유럽의약품청)에서 판매 허가 심사 중이다.
고형광 기자 kohk0101@asiae.co.kr
<ⓒ투자가를 위한 경제콘텐츠 플랫폼, 아시아경제(www.asiae.co.kr) 무단전재 배포금지>

![전문가 4인이 말하는 '의료 생태계의 대전환'[비대면진료의 미래⑥]](https://cwcontent.asiae.co.kr/asiaresize/319/2026013014211022823_1769750471.png)

















![[속보]정부](https://cwcontent.asiae.co.kr/asiaresize/308/2026020414452628585_1770183926.png)


![[속보]'미공개정보 주식거래' LG家 장녀 부부 무죄](https://cwcontent.asiae.co.kr/asiaresize/308/2026020911364534184_1770604605.png)

