강동경희대학교병원, 양산 베데스다병원 IRB승인
[아시아경제 박미주 기자]뇌성마비 환아를 대상으로 자가지방줄기세포의 안전성과 치료효능을 평가하기 위한 임상시험이 시작된다.
네이처셀은 뇌성마비 줄기세포 치료 기술개발을 목표로 강동경희대학교병원과 양산베데스다병원에서 연구자임상시험을 실시하기 위해 식품의약품안전처에 승인 신청을 완료했다고 9일 밝혔다.
뇌성마비는 신경근육계의 결함이 단일 혹은 다발성으로 발생한 미성숙한 뇌의 비진행적 손상의 원인으로 발생하며, 결과적으로 운동기능과 감각통합의 손상이 발생하는 난치병이다.
전 세계적으로 뇌성마비 유병률은 1000명당 1.5~4명 발병한다. 국내의 경우 남아가 1000명당 3.5명, 여아 2.8명으로 평균 3.2명인 것으로 나타났다. 특히 뇌성마비 중요 위험인자인 조산아 생존율이 증가하고 있는 것을 고려할 때 앞으로 뇌성마비 환아 유병률은 점차 증가할 것으로 전망된다.
앞서 알바이오 기술로 배양된 지방유래 중간엽 줄기세포는 독성평가 인증기관인 서울대학교병원 임상의학연구소에서 독성·발암성에 대한 안전성을 평가해 독성이나 종양이 발생하지 않는 것이 확인됐다. 줄기세포 생명재단 후원으로 줄기세포를 체험한 뇌성마비 환아들에서도 개선효과를 관찰했다.
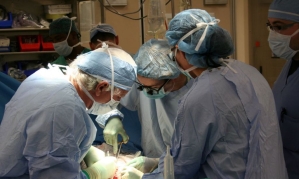
이번 연구는 뇌성마비 환아(3~12세)를 대상으로 지방유래 중간엽 줄기세포를 정맥 내 반복 투여함으로써 손상된 감각·운동기능의 개선과 안전성 확인을 목표로 하고 있다. 본 임상시험은 강동경희대학교병원과 양산베데스다병원에서 진행된다.
이 임상연구는 알바이오에서 줄기세포를 배양해 제공하고 네이처셀이 임상연구에 소요되는 자금을 전액 부담한다. 식약처 승인 후 다음 달부터 환자모집에 들어갈 예정이다.
바이오스타 줄기세포기술원장인 라정찬 박사는 “연구자임상결과에 따라 안전성과 유효성이 추정되면 재생의료기술로서 인정하고 있는 일본에서부터 치료에 적용할 수 있어 국제적으로 많은 뇌성마비 환자들을 도울 수 있을 것"이라고 판단했다.
박미주 기자 beyond@asiae.co.kr
<ⓒ투자가를 위한 경제콘텐츠 플랫폼, 아시아경제(www.asiae.co.kr) 무단전재 배포금지>
![전문가 4인이 말하는 '의료 생태계의 대전환'[비대면진료의 미래⑥]](https://cwcontent.asiae.co.kr/asiaresize/319/2026013014211022823_1769750471.png)














![또 19억 판 아버지, 또 16억 사들인 아들…농심家 '셋째 父子'의 엇갈린 투심[상속자들]](https://cwcontent.asiae.co.kr/asiaresize/308/2026013009165322085_1769732214.jpg)



![쿠팡 잡으려고 대형마트 새벽배송…13년 만의 '변심'에 활짝 웃는 이곳[주末머니]](https://cwcontent.asiae.co.kr/asiaresize/308/2025042307522530624_1745362344.jpg)



