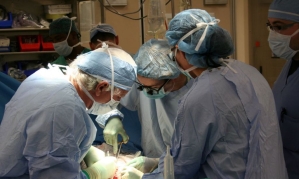
[아시아경제 송화정 기자]크리스탈지노믹스(이하 크리스탈)는 유럽에서 진행 중인 슈퍼박테리아 박멸 신약후보(개발코드명 CG400549)의 임상 1상 후기 시험의 최종 결과 보고서를 정식 수령했다고 18일 공시를 통해 밝혔다.
크리스탈측은 "이번 임상 1상 최종 보고서 수령으로 슈퍼박테리아 박멸 신약후보의 안전성을 공식적으로 평가받았으며 약효를 평가하는 임상 2상 진행을 준비 중"이라면서 "이번에 사람을 대상으로 약물의 안전성이 확인됐고 이미 동물을 통해 약효가 입증된 만큼 임상2상 시험 후 기술수출 협의도 활성화 될 것으로 보인다"고 설명했다. 임상 2상 전기시험은 미국과 유럽의 임상기관들과 협의 중이며 조만간 전체 일정과 비용을 검토하여 계약할 계획이다.
크리스탈이 개발 중인 슈퍼박테리아 신약후보는 사람에게는 없고 박테리아에만 존재하는 특정 질환 표적단백질을 무력화시켜 슈퍼박테리아를 박멸하는 새로운 개념의 치료제로 2026년까지 미국 특허권을 획득했다. 기존의 항생제와는 전혀 다른 새로운 작용기작의 신약후보로 기존의 항생제들이 작용하지 않는 슈퍼박테리아에만 작용할 것으로 크게 기대되는 신약후보다.
임상 2상 진입 예정인 슈퍼박테리아 박멸 신약후보는 이미 임상1상 시험 이전에 진행한 약효평가에서 화이자 제약사의 자이복스 및 제네릭인 반코마이신 약제들에 비해 4배에서 8배 더 우수한 슈퍼박테리아 박멸 효능을 평가 받은 것으로 확인된 바 있다.
송화정 기자 yeekin77@
<ⓒ투자가를 위한 경제콘텐츠 플랫폼, 아시아경제(www.asiae.co.kr) 무단전재 배포금지>
![전문가 4인이 말하는 '의료 생태계의 대전환'[비대면진료의 미래⑥]](https://cwcontent.asiae.co.kr/asiaresize/319/2026013014211022823_1769750471.png)














![또 19억 판 아버지, 또 16억 사들인 아들…농심家 '셋째 父子'의 엇갈린 투심[상속자들]](https://cwcontent.asiae.co.kr/asiaresize/308/2026013009165322085_1769732214.jpg)

![쿠팡 잡으려고 대형마트 새벽배송…13년 만의 '변심'에 활짝 웃는 이곳[주末머니]](https://cwcontent.asiae.co.kr/asiaresize/308/2025042307522530624_1745362344.jpg)

![[속보]소방당국](https://cwcontent.asiae.co.kr/asiaresize/308/2025092623441151167_1758897850.jpg)


