글로벌 42조원 위식도역류질환 시장
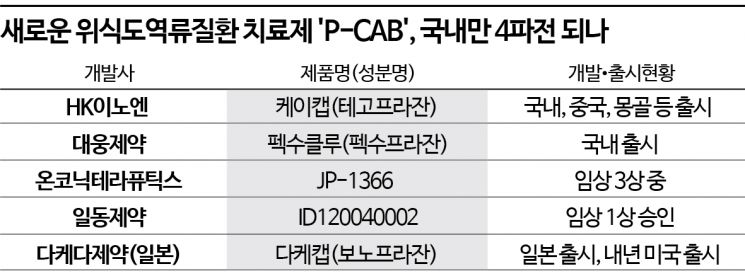
일동제약 개발 가세하면서 국내서만 4파전
HK이노엔 '케이캡'·대웅 '펙수클루' 빠르게 시장 장악
제일 'JP-1366' 연내 임상 마칠듯
[아시아경제 이춘희 기자] 위식도역류질환 치료제 시장에서 '칼륨 경쟁적 위산분비차단제(P-CAB)'의 비중이 급성장하면서 다양한 제약사들이 잇따라 도전장을 던지고 있다. 아직 해외 제약사들의 개발이 미진한만큼 국내 제약사들이 빠르게 해외 시장도 장악해나가는 모습이다.
16일 관련 업계에 따르면 최근 일동제약은 식품의약품안전처로부터 P-CAB 기전의 'ID120040002' 임상 1상 임상시험계획(IND)을 승인받았다. 건강한 성인 남성을 대상으로 ID120040002의 안전성 등을 평가하기 위한 단계적 증량 임상이다. 서울대병원에서 수행된다.
P-CAB 제제는 기존 치료제인 ‘프로톤펌프억제제(PPI)’ 대비 다양한 장점이 부각되며 위식도역류질환 치료 영역에서 각광받고 있다. PPI는 식사 30분 전 약을 복용해야 하고, 위산 분비를 촉진해 야간에 산분비가 일어나는 등의 불편함이 있었다. 골다공증, 뇌졸중 등 부작용도 논란이 됐다. 하지만 P-CAB 제제는 식사 시간에 관계없이 복용할 수 있고, 야간 속쓰림도 개선됐다.
일동제약의 P-CAB 제제 개발 도전도 PPI 제제 시장이 점차 줄어들면서 기존 포트폴리오를 대체하려는 시도라는 분석이 나온다. 일동제약은 올해부터 PPI계열 오리지널 의약품인 아스트라제네카(AZ)의 '넥시움'의 국내 판권을 인수해 영업에 나섰다. 넥시움은 약 10여년간 전 세계 누적 처방량 1위를 기록한 글로벌 블록버스터 의약품이다. 그동안 국내에서는 대웅제약이 판권을 갖고 판매해왔다.
하지만 넥시움의 시장 점유율은 최근 감소세를 보이고 있다. 지난해 넥시움의 원외처방 실적은 482억원으로 전년 대비 13% 줄었다. 처방 실적 1위 타이틀도 한미약품의 '에스메졸'이 538억원으로 22% 성장하면서 빼앗겼다. 이외에도 넥시움의 특허만료 후 다양한 제네릭 제품이 판매되면서 각종 PPI계열 약물들이 시장 점유율 다툼을 벌이고 있다.
반면 P-CAB 제제는 현재 국내에서만 총 5개의 물질이 출시됐거나 본격적 개발 단계에 접어드는 등 급성장하고 있다. 2005년 세계 최초의 P-CAB 제제 약물로 개발된 유한양행의 '레바넥스(성분명 레바프라잔)'이 큰 성과를 거두지 못했지만 2018년 HK이노엔의 '케이캡(테고프라잔)'이 허가를 취득한 데 이어 대웅제약의 '펙수클루(펙수프라잔)'가 지난해 허가를 받으면서 P-CAB 제제가 빠르게 시장을 장악해나가고 있다.
케이캡은 출시 3년 만인 지난해 판매액 1000억원을 넘어섰고, 올해는 1200억원에 달할 것으로 전망된다. 미란성 식도염, 비미란성 식도염, 위궤양, 헬리코박터파일로리 제균, 미란성 위식도역류질환 치료 후 유지요법 등 다양한 적응증을 확보했다. 펙수클루도 지난 7월 출시 이후 3분기 45억원의 매출을 올리며 시장 안착에 나서고 있다.
이외에도 제일약품의 자회사인 온코닉테라퓨틱스에서 'JP-1366'의 임상 3상을 진행 중이다. 역류성 식도염 적응증은 올해 안으로 임상을 끝마칠 전망이고, 위궤양은 지난 6월 3상 IND를 승인받았다.
총 42조원에 달하는 것으로 알려진 글로벌 위식도역류질환 치료제 시장이 P-CAB으로 패러다임 전환이 일어나면서 국내 기업들이 세계 시장을 장악할 수 있을 것이란 기대도 나온다. 아직 다국적 제약사 중 P-CAB 제제를 내놓은 것은 일본 다케다 제약 뿐이다.
다케다의 ‘다케캡(보노프라잔)’은 2019년 국내 허가를 받았지만 이후 출시가 이뤄지지 않고 있는 것과 달리 미국 내 시장 진출은 서두르고 있다. 헬리코박터 제균 요법으로 미국 식품의약국(FDA) 승인을 받은 데 이어 미란성식도염(EE) 치료제로도 FDA에 허가를 신청하고 내년 1월11일로 심사기한을 받았다. 또한 비미란성 위식도역류질환(NERD)에 대해서도 임상 3상을 진행하고 있다. 내년 중 임상을 마칠 계획이다.
지금 뜨는 뉴스
국내 제약사들 역시 해외 진출을 서두르고 있다. HK이노엔은 케이캡의 중국, 몽골 판매를 시작한 데 이어 지난달 미국 파트너사 브레인트리를 통해 위식도역류질환에 대한 미국 임상 3상 IND를 FDA로부터 승인받았다. 대웅제약 역시 미국 협력사 뉴로가스트릭스와 내년 중 미국 3상을 개시할 계획이다. 제일약품은 유럽 3상을 추진하고 있다.
이춘희 기자 spring@asiae.co.kr
<ⓒ투자가를 위한 경제콘텐츠 플랫폼, 아시아경제(www.asiae.co.kr) 무단전재 배포금지>









![전문가 4인이 말하는 '의료 생태계의 대전환'[비대면진료의 미래⑥]](https://cwcontent.asiae.co.kr/asiaresize/319/2026013014211022823_1769750471.png)

















![[내일날씨]설날 아침 영하 추위, 오후엔 풀려…](https://cwcontent.asiae.co.kr/asiaresize/308/2026021309201341738_1770942013.jpg)
