하나금융투자 보고서,
회전근개 질환 치료제 FDA 승인 준비 중
2014년 상장 이후 꾸준히 흑자 기록
[아시아경제 이민지 기자]하나금융투자는 25일 독보적인 세포배양기술을 가진 테고사이언스가 회전근개 치료제의 글로벌 임상 신청으로 높은 성장세가 기대된다는 의견을 내놓았다.
![[클릭 e종목]"테고사이언스, 회전근개 치료제 美 FDA 임상 신청 임박"](https://cphoto.asiae.co.kr/listimglink/1/2014102310322340004_2.jpg) 테고사이언스 로고
테고사이언스 로고
김두현 하나금융투자 연구원은 “테고사이언스는 국내에서 독보적인 세포배양기술을 보유하고 있다"며 “이러한 기술력을 바탕으로 국내에서 허가 받은 세포치료제 15개 중 3개가 이 회사의 것”이라고 설명했다.
세포배양기술은 줄기세포와 재생의학 창시자인 하워드 그린 교수의 그린 배양법을 개량해 사용 중이다. 그린 배양법을 활용해 2~3주 이내에 1cm2의 피부 조직에서 1만cm2이상의 피부 배양이 가능하다.
테고사이언스는 2014년 상장 이후 지금까지 흑자를 기록하고 있다. 수익 대부분은 동종 유래 세포치료제인 칼로덤에서 나온다. 칼로덤은 심부 2도 화상의 재상피화 촉진과 당뇨성족부궤양 상처치유 촉진이라는 두가지 적응증을 가지고 있다. 두 적응증 모두 건강보험 급여 적용이 가능하다.
이외에도 3도 화상 치료제 홀로덤, 주름 개선에 사용되는 로스미르, 기초연구 실험용 피부 모델인 네오덤의 매출도 꾸준히 오르고 있다.
테고사이언스는 국책과제로 선정된 회전근개 질환 치료와 관련해 TPA-114와 TPX-115를 파이프라인으로 두고 있다. TRX-114는 자기 유래 세포를 활용해 전 층 파열을, TRX-115는 동종 유래 세포를 활용해 부분 층 파열에 대응한다.
김두현 연구원은 “현재 TRX-114는 국내 임상 3상 환자를 모집 중이고 TRX-115는 국내 1/2상 IND승인을 받았다”며 “TRX-115는 동종 유래 세포를 활용하기 때문에 완제품 대량 생산이 가능해 2021년 초 미국 식품의약청(FDA) 임상시험 IND 신청도 고려 중이다”고 설명했다.
지금 뜨는 뉴스
이어 그는 “고령화 인구와 레저 스포츠 활동 증가에 따라 회전근개 질환 발병률이 증가할 것”이라며 “세포치료제 수요 증가의 수혜를 누릴 것”이라고 전망했다.
이민지 기자 ming@asiae.co.kr
<ⓒ투자가를 위한 경제콘텐츠 플랫폼, 아시아경제(www.asiae.co.kr) 무단전재 배포금지>
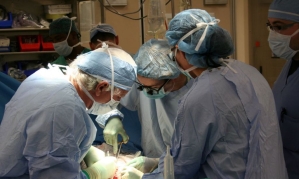
![전문가 4인이 말하는 '의료 생태계의 대전환'[비대면진료의 미래⑥]](https://cwcontent.asiae.co.kr/asiaresize/319/2026013014211022823_1769750471.png)














![또 19억 판 아버지, 또 16억 사들인 아들…농심家 '셋째 父子'의 엇갈린 투심[상속자들]](https://cwcontent.asiae.co.kr/asiaresize/308/2026013009165322085_1769732214.jpg)



![1년새 10배 올랐는데 아직 더 남았다…폭발 성장하는 이 기업[주末머니]](https://cwcontent.asiae.co.kr/asiaresize/308/2026020811051332854_1770516313.png)

![쿠팡 잡으려고 대형마트 새벽배송…13년 만의 '변심'에 활짝 웃는 이곳[주末머니]](https://cwcontent.asiae.co.kr/asiaresize/308/2025042307522530624_1745362344.jpg)
![금·은·비트코인까지 '출렁'…트럼프 선택, 왜 하필 '워시'였나[주末머니]](https://cwcontent.asiae.co.kr/asiaresize/308/2025100509211360399_1759623673.jpg)