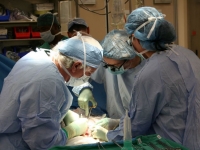
[아시아경제 이창환 기자] 한독은 바이오 벤처기업 제넥신과 공동 개발하는 차세대 성장호르몬(GX-H9)의 유럽 임상 1상 시험이 지난달 30일 완료됐다고 8일 밝혔다.
한독의 임상 전문가와 제넥신의 과학 전문가로 구성된 태스크포스(TF)팀은 작년 8월 유럽 식약청(EMA)에서 임상 승인을 받아 임상개발에 집중해 왔다. 그 결과 당초 예상보다 2달을 단축해 8개월 만에 임상 시험을 종료했다.
이번 임상시험에서 네덜란드의 건강한 성인 남성 32명을 대상으로 평가 한 결과 기존 해외 개발제품 후보들에게 문제가 됐던 투여 부위의 통증, 지방위축증, 항체 생성 등의 부작용이 관찰되지 않았다. 혈액학적, 생화학적 검사 등의 종합적 분석을 통해서 안전하다는 것도 입증됐다.
또한 쥐와 원숭이 실험결과를 통해 예측했던 대로 매일 맞은 1세대 제품에 비해 GX-H9은 30배 이상의 반감기를 보였다. 키 성장에 필수적인 인자 생성도 매우 효율적으로 유도시켰다.
GX-H9는 제넥신의 플랫폼 기술인 ‘항체융합기술(hyFc)’를 융합한 제품이다. 기존 기술과는 달리 성장호르몬에 적용했을 때 활성의 급격한 감소 없이도 반감기가 크게 증가돼 안전하면서도 효능이 장시간 유지되는 차세대 성장호르몬의 특성을 보유했다.
지금 뜨는 뉴스
김영진 한독 회장은 "GX-H9을 효능과 지속력을 겸비한 최고의 성장호르몬 제품으로 개발하기 위해, 한국, 유럽 그리고 미국에서 다국적 임상 2상을 준비 중에 있다"며 "글로벌 대기업을 대상으로 라이선스 아웃 등의 사업화도 본격적으로 착수한다"고 말했다.
성영철 제넥신 대표는 "양사는 임상 2상 이후에 한국 등 아시아에서 임상 3상을 진행한 후 제품의 국내 판매 및 수출도 계획하고 있다"며 "임상개발, 사업개발 그리고 마케팅 전략까지 상호협력을 통해 윈윈 협력 모델을 더욱 강화시킬 예정"이라고 강조했다.
이창환 기자 goldfish@asiae.co.kr
<ⓒ투자가를 위한 경제콘텐츠 플랫폼, 아시아경제(www.asiae.co.kr) 무단전재 배포금지>

![전문가 4인이 말하는 '의료 생태계의 대전환'[비대면진료의 미래⑥]](https://cwcontent.asiae.co.kr/asiaresize/319/2026013014211022823_1769750471.png)