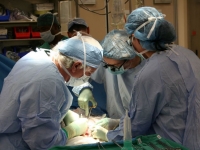
식약청 '임상시험 종합발전계획' 수립
[아시아경제 박혜정 기자]앞으로 임상시험을 수행하는 기관마다 '피험자 보호센터'가 구축되고 의대와 약대 교육과정에는 임상연구 윤리과목이 신설된다. 또 오는 2020년까지 단계적으로 신속승인제를 도입해 임상시험 규제경쟁력을 강화한다.
식품의약품안전청은 임상시험에 참여하는 환자의 안전을 확보하고 중장기적인 임상시험 발전을 위해 이 같은 내용의 '임상시험 종합발전계획'을 수립했다고 10일 밝혔다.
식약청에 따르면 국내 임상시험 승인건수는 2000년 45건에서 2010년 439건으로 10배 가량 늘었다. 최근에는 다국가 임상시험이 활발해지면서 2015년에는 600건, 2020년에는 1000건에 달할 것으로 식약청은 내다보고 있다.
하지만 그동안 임상시험 피험자의 보상이나 안전 관리 체계가 미흡하고, 임상시험 전문인력이 부족하다는 지적이 제기됐었다.
이에 따라 식약청은 올 1월 '임상미래창조 2020 기획단'을 발족하고 10차례 논의를 이어왔다. 그 결과는 ▲피험자 안전보호체계 강화 ▲임상시험 규제경쟁력 강화 ▲임상시험 역량강화 ▲임상시험 소통강화 체계 구축 ▲의료기기 임상시험 발전 방안 등 5대 추진전략으로 도출됐다.
기획단은 우선 피험자의 안전 관리체계를 강화하기 위한 제도를 마련했다.
이를 위해 현재 연세대신촌세브란스병원, 서울대병원·분당서울대병원·보라매병원 등 일부 대형병원에만 있는 '피험자 보호센터'를 임상시험 기관마다 설치해 상시적인 상담 창구를 마련키로 했다.
임상시험 심사위원회(IRB) 인증제를 도입하고 심사위원의 교육 이력을 관리해 임상시험의 적절성을 확보하는 한편, 국내 임상시험 피해자 보상에 대한 규약 표준 권고안을 마련한다는 내용도 포함됐다.
또 임상윤리를 확립하기 위해 의대와 약대 교육과정에 임상연구 윤리과목을 신설키로 했다.
아울러 임상시험 규제경쟁력을 강화하기 위해서 단계적으로 신속승인제를 도입하고 유연한 임상시험 심사시스템을 마련키로 했다. 신속승인제의 경우 1단계로 오는 2013년까지 건강한 성인대상 1상, 시판중인 항암제 연구자 임상시험 등에 적용하고, 2단계(~2020년)로 0·1상, 연구자 임상시험 등으로 확대할 계획이다.
이 밖에 ▲국제표준에 적합한 임상시험자료 전자신청·등록시스템 도입 ▲이상반응 전자보고 시스템 구축 ▲민간 인력에 대한 역량강화 프로그램 마련 및 식약청 전담인력 전문성 강화 ▲국내 임상시험 수준에 대한 해외홍보 및 임상시험계획 데이터베이스(DB)의 정보방 공개 등도 이번 종합계획에 들어있다.
식약청은 "임상시험 피험자 참여에 대한 일반 국민의 부정적인 인식이 이번 종합계획을 통해 긍정적으로 전환될 것으로 전망된다"면서 "임상시험 관련 대국민 인식 전환과 더불어 임상시험 산업 분야가 크게 발전할 것으로 기대한다"고 말했다.
박혜정 기자 parky@
<ⓒ투자가를 위한 경제콘텐츠 플랫폼, 아시아경제(www.asiae.co.kr) 무단전재 배포금지>

![전문가 4인이 말하는 '의료 생태계의 대전환'[비대면진료의 미래⑥]](https://cwcontent.asiae.co.kr/asiaresize/319/2026013014211022823_1769750471.png)