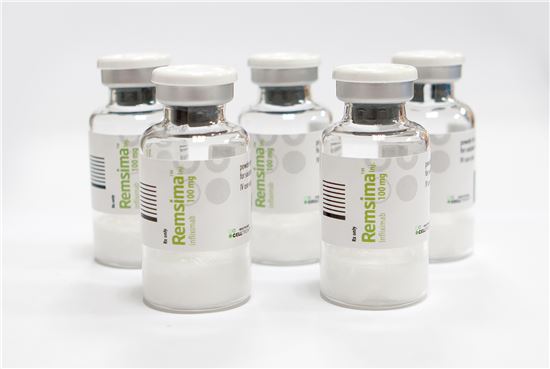
[아시아경제 김보경 기자] 28일 유럽 의약품청(EMA)으로부터 판매 허가를 받은 셀트리온의 항체 바이오시밀러(바이오복제약) '램시마'(Remsima)는 다국적 제약사 존슨앤드존슨(J&J)의 '레미케이드'를 복제한 약이다. 임상시험에서 대조약(레미케이드)과 안전성, 유효성 측면에서 동등함을 입증해 레미케이드와 동일하게 류마티스 관절염, 강직성 척추염, 궤양성 대장염, 크론병, 건선 등에 사용할 수 있다.
단 바이오의약품은 살아있는 생물 세포를 활용하기 때문에 오리지널약과 100% 동일하게 만들 수 없다. 구조적으로 완벽히 같다는 의미에서 '제네릭'(generic)이란 용어를 쓰는 화학 의약품과 달리 '유사하다'는 의미의 '시밀러'(similar)라는 용어를 사용하는 것도 이 때문이다.
램시마는 EMA에서 인정받은 첫 바이오시밀러이자, 글로벌 임상시험을 거쳐 규제 당국이 허가한 세계 최초의 항체 바이오시밀러다. 앞서 인도의 닥터레디(Dr.Reddy)사가 레미케이드를 복제해 자국 내에서 판매하고 있지만, 국제적으로 공인받지 않았다.
램시마에는 제품 개발부터 허가까지 7년 동안 2000억원이 투입됐다. 셀트리온은 지난 2006년 물질 개발을 시작해 지난 2011년 11월 전 세계 20개국 115개 사이트(중복 국가·사이트 제외)에서 총 874명의 환자를 대상으로 진행한 글로벌 임상 1상과 3상시험을 성공적으로 마쳤다. 이후 지난해 3월 EMA에 램시마의 제품 허가를 신청했다. EMA에 제품 허가를 신청한지 2년 3개월 만에 승인 획득에 성공한 것이다. 유럽 판매허가에 앞서 지난해 7월 식품의약품안전처로부터 국내 판매 허가를 받았다.
램시마의 명칭에도 의미가 있다. '램(REM)'은 류마티스 관절염(Rheumatoid arthritis)을 뜻하고 '시마(SIMA)'는 항체의약품 바이오시밀러(biosimilar&mabs)를 의미한다. 주 성분인 인플릭시맙(infliximab)은 지난 1998년 발매 이후 150만명 이상에게 사용돼온 자가면역질환 치료제지만, 레미케이드 1병에 55만원(램시마 판매 전)에 달할 정도로 상대적으로 고가였다. 때문에 보험급여를 제공하는 정부와 환자의 재정 상태에 따라 실제 이 약을 필요로 하는 환자들의 상당수는 사용하지 못했다. 램시마의 등장은 다국적 제약사의 독점구조를 깨고 환자 부담을 줄여주는 효과가 있다.
김보경 기자 bkly477@
<ⓒ투자가를 위한 경제콘텐츠 플랫폼, 아시아경제(www.asiae.co.kr) 무단전재 배포금지>
![전문가 4인이 말하는 '의료 생태계의 대전환'[비대면진료의 미래⑥]](https://cwcontent.asiae.co.kr/asiaresize/319/2026013014211022823_1769750471.png)














![또 19억 판 아버지, 또 16억 사들인 아들…농심家 '셋째 父子'의 엇갈린 투심[상속자들]](https://cwcontent.asiae.co.kr/asiaresize/308/2026013009165322085_1769732214.jpg)



![쿠팡 잡으려고 대형마트 새벽배송…13년 만의 '변심'에 활짝 웃는 이곳[주末머니]](https://cwcontent.asiae.co.kr/asiaresize/308/2025042307522530624_1745362344.jpg)


