로슈 '간테네루맙' 3상 실패
6~8% 개선 확인… 통계 입증은 못 해
15년 프로젝트 결국 좌초되나
바이오젠·에자이 '레카네맙' 3상 성공
내년 1월 FDA 승인 판가름
릴리 '도나네맙' 임상 3상 중
국내서도 젬백스·아리바이오·지엔티파마 도전
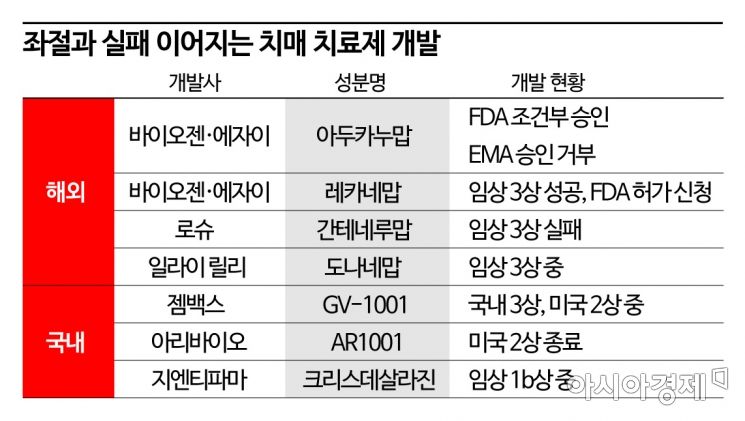
[아시아경제 이춘희 기자] 성공하는 듯 보였던 치매 정복의 꿈이 또 다시 좌절을 겪었다. '아두헬름(성분명 아두카누맙)'의 실패를 겪었던 바이오젠과 에자이가 '레카네맙'의 임상에 성공하며 치매 치료제 개발이 다시 탄력을 받는 듯 했지만 로슈의 '간테네루맙'이 다시 3상에서 고배를 마셨다.
14일(현지시간) 로슈는 간테네루맙의 초기 알츠하이머성 치매 환자 대상 임상 3상 'GRADUATE' 연구의 톱 라인을 중간 분석한 결과 1차 유효성 지표 입증에 실패했다고 밝혔다. 간테네루맙은 로슈와 자회사인 제넨텍이 독일 모포시스로부터 기술 도입해 개발 중인 아밀로이드-베타(Aβ) 표적의 알츠하이머성 치매 항체 치료제다. 특히 아두헬름과 레카네맙, 일라이 릴리의 '도나네맙' 등 정맥주사(IV)인 다른 치료제들과 달리 피하주사(SC) 제형으로 투약 편의성을 높여 기대를 모으기도 했다.
하지만 로슈는 'GRADUATE 1'(982명), 'GRADUATE 2'(1016명)이라는 이름으로 나눠 진행된 이번 임상 3상에서 1차 목표의 통계적 유의성 충족에 실패했다고 밝혔다. 임상 1차 목표는 약 2년(116주) 후 '임상치매척도(CDR-SOB)'의 기준선 대비 변화 정도였다.
이 결과 위약군 대비 6~8%의 추가적인 CDR-SOB 개선이 확인됐다. 하지만 우연이 아닌 실제 간테네루맙의 약효에 의한 것임을 확인하기 위한 'P값(유의확률)' 입증에는 실패했다.
이로써 로슈가 15년가량 이끌어왔던 간테네루맙의 임상은 또 다시 좌절됐다. 간테네루맙은 2014년에도 경도~중등도 알츠하이머 환자를 대상으로 임상 3상이 이뤄졌지만 실패했다. 적응증을 경도인지장애(MCI) 또는 경도 알츠하이머 환자로 변경해 재도전했지만 또 고배를 마셨다.
다만 로슈가 간테네루맙과 관련한 다양한 추가 개발을 이어가고 있어 전면 개발 중단으로 이어질 가능성은 크지 않다. 이번 'GRADUATE' 임상 외에도 인지 저하가 아직 나타나진 않았지만 Aβ 축적 징후가 있는 이들을 대상으로 한 예방임상인 'SKYLINE' 임상 3상을 1200명 대상으로 추진하는 한편 혈뇌장벽(BBB) 투과를 높이기 위해 뇌셔틀을 붙인 이중항체 'RG6102'의 임상 1상도 진행하고 있기 때문이다.
간테네루맙의 실패로 바이오젠과 에자이의 아두헬름이 시장 진출에 실패했지만 레카네맙이 임상 3상에서 약효를 입증해내면서 되살아나는 듯 했던 치매 정복의 기대감도 다소 꺾이게 됐다. 지난 9월 바이오젠과 에자이는 공동 개발하고 있는 레카네맙의 글로벌 임상 3상 1차 유효성 지표 달성에 성공했다. 투약 18개월 후 CDR-SOB의 기준선 대비 개선 정도를 지표로 설정한 가운데 위약군 대비 27%의 개선 효과를 입증했다. 통계적 유의성도 확인됐다.
이로써 양측의 희비는 엇갈리게 됐다. 특히 두 연구결과 모두 오는 29일~다음달 2일 미국 샌프란시스코에서 열리는 알츠하이머 임상시험(CTAD) 국제 콘퍼런스에서 발표될 계획인만큼 극명한 대조가 이뤄지게 됐다. 레카네맙은 승인에도 탄력을 받고 있다. 지난 7월 미국 식품의약국(FDA)로부터 생물학적 제제 허가신청서(BLA)를 승인받은 상태로 내년 1월6일 전에 승인 여부가 판가름될 예정이다. 바이오젠과 에자이는 이외에도 유럽과 일본에 승인을 신청할 계획이다.
두 약의 임상 3상 결과가 잇따라 나오면서 시장은 다음 타자로 일라이 릴리의 '도나네맙'을 주목하고 있다. 현재 임상 3상 중으로 내년 상반기 안으로 임상이 마무리될 전망이다. 임상 2상에서 통합 알츠하이머 평가척도(iADRS)에서 위약군 대비 32%의 개선 효과를 보인 바 있다.
국내에서도 치료제 개발 시도는 이어지고 있다. 젬백스, 아리바이오, 지엔티파마 등이 나선 가운데 대부분 Aβ나 타우가 아닌 신경염증 제거, 복합 기전을 추구하고 있다. 젬백스는 ‘GV1001’의 국내 3상과 미국 등 글로벌 2상을 추진중이다. 2상은 미국과 유럽 7개국(스페인, 프랑스, 이탈리아, 포르투갈, 네덜란드, 폴란드, 핀란드) 동시 진행을 계획 중으로 미국과 스페인에서는 임상시험계획(IND)을 승인받았다.
지금 뜨는 뉴스
경구용 치료제 ‘AR1001’을 개발하고 있는 아리바이오는 글로벌 임상 3상 진입을 위한 IND를 FDA에 제출한 상태다. 반려견 인지기능장애증후군(CDS) '제다큐어'로 상용화된 성분을 인체에 적용하는 ‘크리스데살라진’을 개발하고 있는 지엔티파마는 임상 1상을 마쳤다.
이춘희 기자 spring@asiae.co.kr
<ⓒ투자가를 위한 경제콘텐츠 플랫폼, 아시아경제(www.asiae.co.kr) 무단전재 배포금지>









![전문가 4인이 말하는 '의료 생태계의 대전환'[비대면진료의 미래⑥]](https://cwcontent.asiae.co.kr/asiaresize/319/2026013014211022823_1769750471.png)